【FDA美國代理人】什么是FDA美國代理人
- 時間:2021-04-28作者:上海沙格企業管理咨詢有限公司瀏覽:226
上海沙格企業管理咨詢有限公司專注于FDA510K認證,歐盟自由銷售證書,MDR認證,ISO13485認證,MHRA注冊,英國授權代表,UKCA認證,瑞士代表,CH,REP,FDA驗廠輔導等, 歡迎致電 13818104617
詞條
詞條說明
ISO13485認證適用范圍本標準適用于進行醫療器械的設計和開發、生產、安裝和服務或相關服務的設計、開發和提供等相關行業。在標準中定義的醫療器械指:制造商的預期用途是為下列一個或多個特定目的用于人類的,不論單獨使用或組合使用的儀器、設備、器具、機器、用具、植入物、體外試劑或校準器、軟件、材料或者其他相似或相關物品。這些目的是:――疾病的診斷、預防、監護、治療或者緩解;――損傷的診斷、監護、治療、緩
醫療器械澳大利亞T GA注冊一)在澳大利亞供應醫療器械程序,如果醫療器械是在海外制造的(即I類消毒; I類測量; II a類; II b類,III類,AI MD類)制造商從T GA或歐盟的認證機構獲得合格評定證據制造商準備澳大利亞符合性聲明主辦者向T GA提交制造商的證據主辦者遞交在AR T G登記申請在AR T G登記后主辦者可以在澳大利亞供應器械器械上市后持續監控二)在澳大利亞供應醫療器械程序
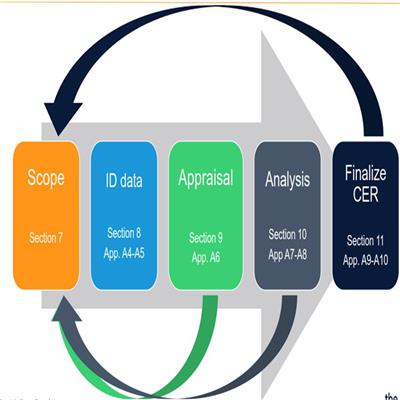
為河南駝人提供IIb類的CE四版臨床評價報告MEDDEV 2.7.1 Rev 4
始建于1993年,前身是“新鄉市駝人醫療器械有限公司”,1994年生產出中國的一支國產PVC氣管插管。研制的氣管導管,獲得河南省技術成果榮譽,填補了國內氣管導管生產的空白。現已擁有13家下屬子公司(其中一家福利企業)、五個生產經營場所(其中三個生產基地)、總占地面積已達690畝。公司員工已近4000人,其中研究生80人,本科生596人,對口率80%。現已安排殘疾職工近500余人;成為生產麻醉、疼
醫療器械美國FDA 510(k)認證簡介 為了在美國上市醫療器械,制造商必須經過兩個評估過程其中之一:上市前通知書[510(k)](如果沒有被510(k)赦免),或者上市前批準(PMA)。 大多數在美國進行商業分銷的醫療器械都是通過上市前通知書[510(k)]的形式得到批準的。在某些情況下,在1976年5月28日之前合法上市的器械,既不要求遞交510(k)也不要求遞交PMA。 510(k)文件是
聯系方式 聯系我時,請告知來自八方資源網!
公司名: 上海沙格企業管理咨詢有限公司
聯系人: 袁玲
電 話: 13818104617
手 機: 13818104617
微 信: 13818104617
地 址: 上海浦東陸家嘴世紀大道1500號
郵 編:
網 址: sungoyuan.b2b168.com
相關推薦
相關閱讀
1、本信息由八方資源網用戶發布,八方資源網不介入任何交易過程,請自行甄別其真實性及合法性;
2、跟進信息之前,請仔細核驗對方資質,所有預付定金或付款至個人賬戶的行為,均存在詐騙風險,請提高警惕!
- 聯系方式
公司名: 上海沙格企業管理咨詢有限公司
聯系人: 袁玲
手 機: 13818104617
電 話: 13818104617
地 址: 上海浦東陸家嘴世紀大道1500號
郵 編:
網 址: sungoyuan.b2b168.com
- 相關企業
- 遼寧中益嘉泰拍賣有限公司
- 杭州安恒達管理咨詢有限公司
- 鄭州林奧企業管理咨詢有限公司
- 天津博雋供應鏈管理有限公司
- 成都思培安信息技術有限公司
- 江蘇凡睿管理咨詢有限公司
- 湖北華思企業管理有限公司
- 北京宏易管理咨詢有限公司
- 重慶博視知識產權服務有限公司
- 青島劉小幫企業管理咨詢有限公司
- 商家產品系列
- 技術咨詢
- 市場調研
- 咨詢
- 產品檢測服務
- 一體化氣浮機咨詢
- 心理咨詢師報名條件
- 心理咨詢師培訓中心
- 心理咨詢師輔導
- 二級心理咨詢師工資
- 電商策劃咨詢
- 咨詢NM500耐磨板
- 山西心理咨詢名師
- 廣州天河財務咨詢
- 天河財務咨詢
- 天河財務咨詢公司
- 廣州財務咨詢
- 廣州財務咨詢公司
- 室內環保咨詢服務
- 煙臺裝修咨詢
- 皮帶輸送機咨詢
- 企業秀咨詢華企立方張小姐
- 土工膜價格咨詢
- 武漢環保咨詢公司
- 西北工業大學在線咨詢報名
- 四川法律援助咨詢平臺
- 薩提亞心理咨詢機構
- 薩提亞心理咨詢工作坊
- 薩提亞心理咨詢師
- 薩提亞心理咨詢工作室
- 鋼化玻璃咨詢廠家
- 產品推薦
- 資訊推薦